Un hydratant thérapeutique parfumé doux, qui procure des bienfaits à la barrière cutanée
(A Scented Therapeutic Moisturizer That Is Mild and Provides Skin Barrier Benefits)
Michelle Garay, Wen-Hwa Li, Xinni Chen, Olha Ilnytska, Ramine Parsa, Simarna Kaur, Michael Southall, Johnson & Johnson Skin Research Center, Johnson & Johnson Consumer Inc., Skillman, NJ, USA
RÉSUMÉ
- Les parfums sont généralement considérés comme des irritants potentiels, pouvant induire des réactions inflammatoires cutanées chez les sujets dont la peau est très sèche, sensible ou compromise. Par conséquent, les dermatologues recommandent souvent l’utilisation d’hydratants thérapeutiques non parfumés aux patients à la peau sensible ou compromise, ce qui peut entraîner une mauvaise observance du traitement. Un hydratant thérapeutique contenant un parfum non irritant pour la peau pourrait fournir aux cliniciens des options à recommander aux patients pour améliorer l’observance.
- Une série de parfums ont été évalués in vitro pour leur potentiel d’inflammation ou d’irritation au niveau des cellules cutanées, et les parfums de noix de coco et de camomille se sont révélés très doux et non irritants. En effet, les crèmes hydratantes aux parfums de noix de coco et de camomille se sont révélées aussi douces que les crèmes hydratantes non parfumées.
- De plus, les hydratants thérapeutiques parfumés ont induit des niveaux similaires d’expression des gènes associés à la barrière cutanée.
- L’ensemble de ces résultats démontre que cet hydratant parfumé est aussi doux qu’une lotion non parfumée et qu’il peut également induire l’expression de plusieurs gènes jouant un rôle dans la fonction barrière de la peau.
OBJECTIFS
- Évaluer le potentiel d’inflammation et d’irritation de deux parfums doux (camomille et noix de coco) au moyen de cellules cutanées in vitro.
- Les hydratants thérapeutiques parfumés ont été évalués en profondeur pour leurs effets in vitro sur : – la barrière cutanée – l’expression des gènes liés à la fonction barrière de l’épiderme.
CONCEPTION DE L’ÉTUDE
- On a utilisé une culture de kératinocytes humains pour évaluer les effets inflammatoires des parfums :
- Sur les interleukines (IL)-1α et IL-8, mesurées par la méthode immunoenzymatique (ELISA).
- Des équivalents de tissus épidermiques MatTek (Ashland, MA, USA) ont été utilisés pour comparer les effets des lotions parfumées et d’une lotion non parfumée sur l’intégrité de la barrière, l’expression génique et l’irritation cutanée :
- Les tissus ont subi un traitement topique au moyen de 6 µl de lotion pendant 24 ou 48 heures.
- L’intégrité de la barrière a été mesurée par résistance électrique transépidermique et celle des cytokines inflammatoires IL-1α et IL-8, par la méthode ELISA.
RÉSULTATS
Figure 1a. Le parfum de camomille n’a induit aucune libération d’IL-1α et d’IL-8 dans les kératinocytes humains
8.7_figure_1.jpg
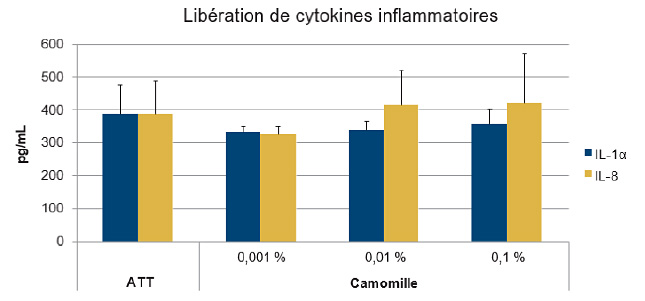
La mesure des cytokines inflammatoires, IL-1α et IL-8, libérées dans les cultures de kératinocytes humains a démontré que le parfum de camomille n’a pas induit de réponse inflammatoire aux doses testées. ATT, aucun traitement témoin.
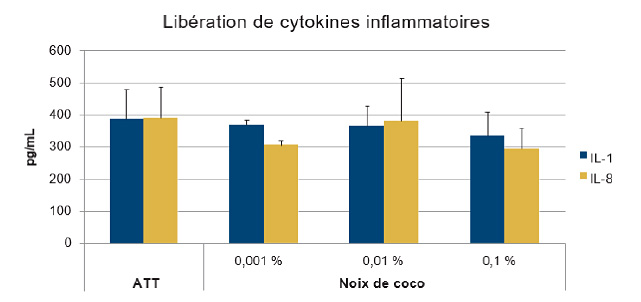
Figure 1b. Le parfum de noix de coco n’a induit aucune libération d’IL-1α et d’IL-8 dans les kératinocytes humains
8.7_figure_1b.jpg
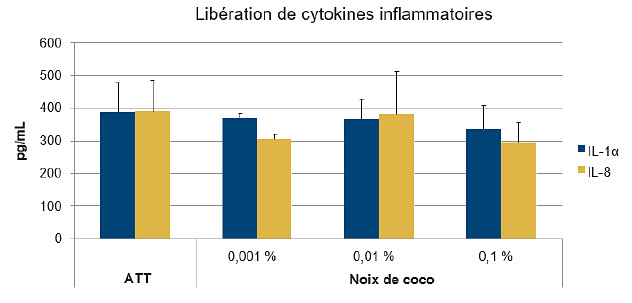
La mesure des cytokines inflammatoires, IL-1α et IL-8, libérées dans les cultures de kératinocytes humains a démontré que le parfum de noix de coco n’a pas induit de réponse inflammatoire aux doses testées. ATT, aucun traitement témoin.
Figure 2a. Dans des équivalents épidermiques humains, les hydratants parfumés ont eu des effets sur la barrière cutanée semblables à ceux produits par l’hydratant parfumé
8.7_figure_2.jpg
Les hydratants au parfum de noix de coco ou de camomille ont entraîné des changements similaires à ceux produits par l’hydratant non parfumé, tel que mesurés par résistance électrique transépidermique.
Figure 2b. De façon semblable aux hydratants non parfumés, les hydratants parfumés n’ont pas accru la libération des médiateurs de l’inflammation
8.7_figure_2b.jpg
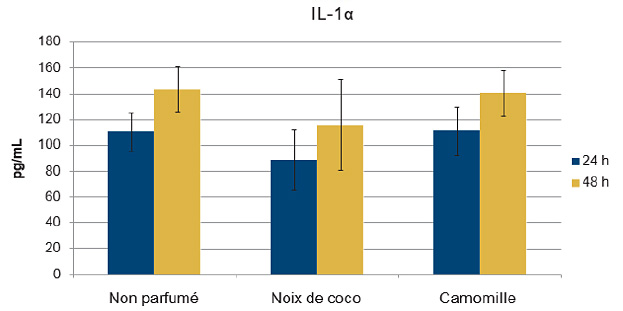
L’hydratant non parfumé et les hydratants au parfum de noix de coco ou de camomille ont induit une libération d’IL-1α semblable dans des équivalents épidermiques humains exposés à ces produits pendant 24 ou 48 heures.
Figure 2c. De façon semblable aux hydratants non parfumés, les hydratants parfumés n’ont pas accru la libération des médiateurs de l’inflammation
8.7_figure_2c.jpg
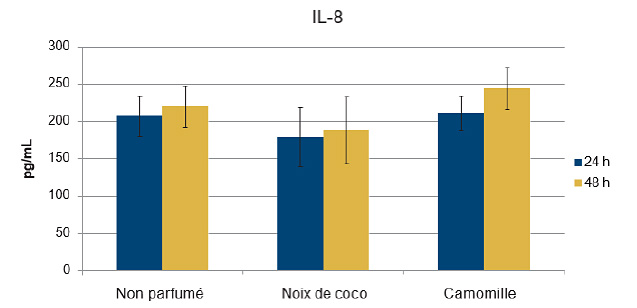
Les hydratants au parfum de noix de coco ou de camomille ont induit une libération d’IL-8 semblable à celle induite par un hydratant non parfumé.
Figure 3. Les hydratants parfumés ont eu un effet semblable à celui des hydratants non parfumés sur l’expression des gènes liés à la barrière cutanée
8.7_figure_3.jpg
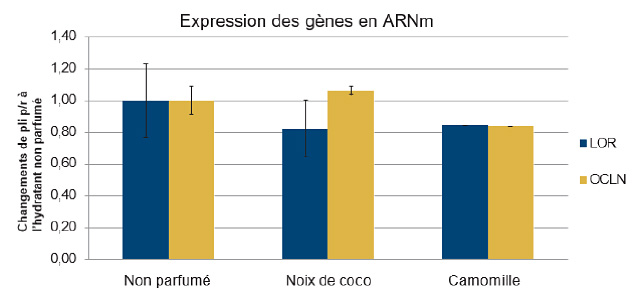
Dans des équivalents épidermiques humains, les hydratants au parfum de noix de coco ou de camomille ont induit des niveaux d’expression des gènes liés à la barrière cutanée (loricrine et occludine) similaires à ceux de l’hydratant non parfumé.
CONCLUSIONS
- Les parfums de noix de coco et de camomille se sont révélés très doux et non irritants.
- Les hydratants au parfum de noix de coco ou de camomille se sont révélés aussi doux que l’hydratant non parfumé.
- Les hydratants parfumés ont un profil d’expression des gènes liés à la barrière cutanée similaire à celui de l’hydratant non parfumé.
- Les hydratants thérapeutiques parfumés, doux et non irritants peuvent offrir aux cliniciens des options de traitement supplémentaires et favoriser une meilleure observance.
DIVULGATIONS
- Michelle Garay, Wen-Hwa Li, Xinni Chen, Olha Ilnytska, Ramine Parsa, Simarna Kaur et Michael Southall sont des employés de Johnson & Johnson Consumer Inc. ou étaient employés de l’entreprise lors de la tenue de ces expériences.
- Cette étude a été financée par Johnson & Johnson Consumer Inc. (Skillman, NJ, États-Unis).
- L’assistance à l’édition, financée par Johnson & Johnson Consumer Inc., a été fournie par Alex Loeb d’Evidence Scientific Solutions (Philadelphie, Pennsylvanie, États-Unis).